Соотношение объемных и микроциркуляторных показателей кровотока у пациентов с эссенциальной артериальной гипертензией
ГОУ ВПО Нижегородская государственная медицинская академия,
НУЗ ДКБ «Дорожная клиническая больница на станции Горький ОАО «РЖД»
Сердечно-сосудистые заболевания наносят значительный ущерб здоровью населения, являясь по данным ВОЗ, наиболее частой причиной смерти, инвалидности и экономических потерь в развитых странах [1].
Одним из наиболее распространенных заболеваний в высокоразвитых странах стала эссенциальная артериальная гипертензия (ЭАГ). Ее эпидемиологическое значение возрастает в виду того, что ЭАГ, как правило, становится инициатором и акселератором других сердечно-сосудистых заболеваний, их ранним и еще поддающимся лечебному контролю предиктором. [2] Одна из причин нарушения стабильности функционального состояния системы кровообращения при ЭАГ - постепенно накапливающиеся изменения артерий и микроциркуляторного русла. Если уплотнение аорты становится важным фактором только с возрастом и на поздних стадиях ЭАГ. то вазоспастические реакции и гипертрофия гладкомышечных клеток сосудистой стенки имеют значение с самого начала формирования заболевания. Структурно-функциональное моделирование резистивных артерий, которое исходно обусловлено адаптацией к повышению АД, необходимостью ограничить избыточную перфузию тканей и защитить от давления микроциркуляторное русло, позже становится ведущим механизмом поддержания постоянно высокого давления. Происходит гипертрофия интимы и меди артерий, изменяется соотношения активно уменьшающегося просвета и возрастающей толщины стенки сосуда [2,3].
В настоящее время принятые в повседневной клинической практике методы оценки центральной гемодинамики не обеспечивают достаточно достоверного контроля ряда показателей наиболее важного звена системы кровообращения - периферического. Сравнительно недавно, в 1984 г., был предложен новый метод изучения микроциркуляции - лазерная допплеровская флуометрия {ЛДФ). ЛДФ основывается на том, что направленный на ткань световой (лазерный) луч рассеивается в ее статических и подвижных компонентах. Отраженный от подвижных частиц световой сигнал имеет допплеровское смещение относительно зондируемого сигнала. Регистрируемый при ЛДФ сигнал количественно характеризует кровоток в микрососудах (артериолы, капилляры, венулы) с временным разрешением около 100 мс и пространственным разрешением 1 мм. Это означает, что ЛДФ дает интегральную информацию, усредняемую по очень большому количеству эритроцитов (примерно 10000). Следует подчеркнуть, что ЛДФ в настоящее время является единственным методом, позволяющим анализировать капиллярную гемодинамику в реальном масштабе времени [4].
В последнее время, в литературных источниках встречаются работы, связанные с
исследованием системы кровообращения методом объемной компрессионной
осциллометрии с использованием прибора АПКО-8-РИЦ. Принципиальным отличием ОКО
от других осциллометрических методов является сохранение низкочастотных составляющих
пульсовой волны. Поскольку стенки артерий после компрессии и кратковременной ишемии
дистального участка конечности изменяют свои характеристики, регистрация ОКО
проводится в режиме набора давления в манжете.
Целью настоящей работы явилась оценка состояния микроциркуляторного русла методом
ЛДФ и его значения в формировании гемодинамических нарушений у пациентов с
эссенциальной артериальной гипертензией.
Материалы и методы
В исследование включены данные по 60 амбулаторным и стационарным пациентам с эссенциальной артериальной гипертензией 1-Й стадии (24 мужчин, 36 женщин) в возрасте от 23 до 63 лет (средний возраст 47.74 ± 9,94 лет). I стадия ЭАГ установлена у 15 пациентов (7 мужчин, 8 женщин) в возрасте от 23 до 55 лет (средний возраст 43,18 ± 11.55 лет), II стадия ЭАГ - у 45 пациентов (17 мужчин, 28 женщин) в возрасте от 24 до 63 лет (средний возраст 49,93 ± 9,34 лет).
Всем исследуемым было выполнено:
• суточное мониторирование АД (СМАД) с помощью монитора «А&О - ТМ2124» по стандартной методике [5]
• ЭХОКГ на аппарате ультразвуковой диагностики Рhilips HDI 1500
• Обследование с целью исключения симптоматической артериальной гипертензии
• Лазерная допплеровская флуометрия
• Объемная компрессионная осциллометрия
Критериями исключения являлись: наличие у пациентов симптоматической артериальной гипертензии, ассоциированных клинических состояний (мозговой инсульт, инфаркт миокарда, сердечная недостаточность выше II ФК, почечная и печеночная недостаточность, сахарный диабет), хронической обструктивной болезни легких, облитерирующих поражений магистральных сосудов, нарушений ритма сердца высоких градаций. На протяжении 3 дней до исследования пациентам были отменены получаемые ими ранее препараты. В случае резкого повышения АД или угрозы возникновения гипертонического криза назначались препараты короткого действия (капотен или клофелин, или нифедипин сублингвально).
Контрольную группу составили 20 практически здоровых добровольцев (6 мужчины, 14 женщин) в возрасте от 22 до 61 лет (средний возраст 46,72 ± 13.75).
Состояние микроциркуляции изучали методом ЛДФ на аппарате «ЛАКК-01» (НПП «ЛАЗМА», 1999г.) в области задней (наружной) поверхности левого предплечья в точке, отстоящей выше основания шиловидных отростков локтевой и лучевой костей на 4 см по срединной линии (зона Захарьина-Геда сердца). Исследование проводилось в дневные часы через 2 часа после приема пищи с предварительной адаптацией к температуре в помещении 20-22°С при положении пациента сидя, левое предплечье расположено на столе на уровне сердца. Производилась запись показателей микроциркуляции в состоянии покоя в течение 3 минут, затем выполнялась окклюзионная проба. Исходная ЛДФ-грамма подвергалась компьютерной обработке, в ходе которой вычислялся средний показатель микроциркуляции (ПМ), коэффициент вариабельности ПМ (Ку), амплитуды колебаний в отдельных частотных диапазонах. Окклюзионная проба проводилась следующим образом: датчиком на конечности регистрировался исходный ПМ, после чего накачивался воздух а предварительно наложенную на плечо манжетку сфигмоманометра. Сила сдавления составляла не менее 250 мм рт ст, продолжительность окклюзии - 3 мин. После чего регистрировалось изменение ПМ в течение 6 минут. По результатам окклюзионной пробы учитывался максимальный показатель реактивной гиперемии (ПМтах) - пиковый ПМ, возникающий после окклюзии, состояние исходного кровенаполнения микроциркуляторного русла или резерв оттока (РО), резерв капиллярного кровотока (РКК) [4].
Исследование показателей гемодинамики методом объемной компрессионной осциллометрии (ОКО) проводилось с использованием аппарата АПКО-8-РИЦ. Проводилось 3 измерения с интервалом в 5 минут с последующим расчетом средних величин следующих показателей: систолическое и диастолическое АД, минутный объем, сердечный индекс, ударный объем крови, ударный индекс, общее и удельное периферическое сопротивление, диаметр артерий, модуль упругости артерий, линейная скорость кровотока [5].
Полученные данные были занесены в электронную базу данных Microsoft Ехсеl 2003. Обработка результатов осуществлялась с помощью статистической программы STATGRAPHIC Plus 5.1. Достоверность различий двух сравниваемых величин определялась по критерию Вилкоксона. Полученные результаты представлены в виде М + Sоl. Также использовался канонический корреляционный анализ.
Результаты и обсуждение
При обработке результатов ЛДФ были получены следующие результаты; у пациентов ЭАГ II стадии по сравнению со здоровыми лицами ПМ выявлено достоверное снижение ПМ, амплитуды медленных (собственных) колебаний , преимущественно за счет миогенного компонента, снижение максимального показателя реактивной гиперемии, резерва оттока и резерва капиллярного кровотока. У пациентов ЭАГ 1 стадии также снижены ПМ, ПМмак по сравнению с здоровыми, однако резервы оттока и капиллярного кровотока в данной группе находятся в пределах нормальных значений. Кроме того у пациентов с ЭАГ повышен коэффициент вариабельности ПМ в сравнении со здоровыми лицами и пациентами ЭАГ II стадии (см. таблица 1).
Таблица 1. Показатели микроциркуляции у больных эссенциальной артериальной гипертензией (ЭАГ) 1-П стадии в сравнении с контрольной группой.
|
ЭАГ I стадии |
ЭАГ II стадии |
Группа контроля |
ПМ (перфузионные единицы, ПЕ) |
3,75±1,20** | 3,93±1,37** | 5,15±2,06* |
Ку (%) |
15,21±8,87** | 10,51±4,6* | 11,99±5,47* |
Амплитуда LF (ПЕ) |
0,74±0,05 | 0,57±0,04*'** | 0.73±0,05 |
ПМмак (ПЕ) |
10,15±1,85** | 8,09±2,99*'** | 12,78±3,79* |
РО (ПЕ) |
1,79±0.20 | 1,08±0,26*'** | 1,55±0,50 |
РКК (%) |
290,81±37,23 | 217,75±45,04*'** | 260,57±36,05 |
(* - р < 0,05 по сравнению с 1 группой, ** - р < 0,05 по сравнению с контрольной группой)
Анализ данных ОКО выявил достоверное повышение общего и удельного периферического сопротивления у пациентов ЭАГ по сравнению с группой контроля, значимое снижение модуля упругости сосудов при II стадии ЭАГ (р=0,02 по сравнению с группой контроля, р=0,04 по сравнению с группой ЭАГ I стадии) (см. таблицу 2).
Таблица 2. Показатели гемодинамики методом ОКО у больных эссенциальной артериальной гипертензией (ЭАГ) 1-П стадии в сравнении с контрольной группой.
|
ЭАГ I стадии |
ЭАГ II стадии |
Группа контроля |
САД (мм рт ст) |
136,36±20,91** | 145,18+20,74** | 123,64+10,61 |
ДАД (мм рт ст) |
81,90+12,07** | 79,89+12,49** | 64,27+8,31* |
ОПСС (дин*см°*сек) |
1817,48+228,27** | 1916,27±267,90** | 1614,38±И5,76* |
УПСС (уел, ед.) |
23,09+6,27 | 31,82+7,02*',** | 26,82+6,05 |
Модуль упругости |
70,09+20,63 | 56,90+16,62*,'** | 72,14+19,23 |
(* - р < 0,05 по сравнению с 1 группой, ** - р < 0,05 по сравнению с контрольной группой)
Полученные данные можно интерпретировать, исходя из сопоставления факторов, влияющих на ЛДФ-сигнал, и известных данных о прогрессирующих по мере развития ЭАГ морфологических изменений микрососудистого русла. На начальном этапе формирования ЭАГ увеличивается сердечный выброс, при этом уменьшение сопротивления в сосудистом русле и давления на капиллярную стенку возможно за счет открытия нефункционирующих капилляров, вследствие чего увеличивается объемная скорость кровотока и повышается вазомоторная активность сосудов микроциркуляторного русла, а на ЛДФ-грамме регистрируется повышенная вариабельность микрососудистого кровотока [7]. При длительном воздействии высокого сердечного выброса на капиллярную сеть происходит уменьшение просвета сосудов вплоть до полного закрытия их просвета за счет сокращения прекапиллярных сфинктеров, демпфирирующих давление на стенки капилляров. В последующем происходит процесс запустевания и разрежения (рарефикации) капилляров и мелких артериол (вначале функциональный, затем структурный). Этот процесс выражается в снижении ПМ, амплитуды LF, ПМмак, РО, РКК по данным ЛДФ и повышении общего и удельного периферического сопротивления, снижении упругости сосудов по данным ОКО при ЭАГ II стадии.
Тесную взаимосвязь между состоянием микроциркуляторного русла и показателями гемодинамики демонстрирует канонический корреляционный анализ: коэффициент корреляции линейных канонических комбинаций 0,71. уровень значимости (р) равен 0.0039 (см. рисунок 1).
Рисунок 1. Диаграмма рассеивания на плоскости первых канонических направлений.
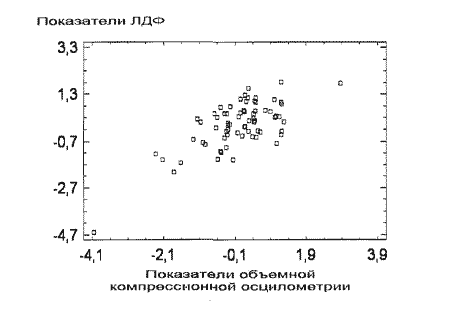
У пациентов с ЭАГ наблюдаются существенные изменения в состоянии микроциркуляторного русла: изменение степени кровенаполнения и скорости кровотока в капиллярном русле, нарушения соотношения колебательных процессов, снижение реактивности сосудов в ответ на окклюзию. При повышении стадии ЭАГ прогрессивно снижается капиллярный кровоток, повышается ОПСС (вне зависимости от уровня ДАД). Использование методов ОКО и ЛДФ дает возможность комплексно оценить состояние периферического кровотока у пациентов с ЭАГ, что позволит более рационально подходить к выбору гипотензивной терапии.
Список литературы
1. Профилактика, диагностика и лечение артериальной гипертензии. Российские
рекомендации. М., 2004.
2. Гогин Е.Е.. Седов В.П. Неинвазивная инструментальная диагностика центрального, периферического и мозгового кровообращения при гипертонической болезни. Терапевтический архив. - 1999. - №4.-С.5-10.
3. Кар1ап N. Нурег1епйюп, гшспхлгсшагюп апё ог§ап о!ата§е. 1лрршсой ШНат5&УИкт5. - 2002. - 116с.
4. Маколкин В.И, Подзолков В.И., Павлов В.И., Богданова Э. А., Камшилина Л.С., Самойленко В.В. Состояние микроциркуляции при гипертонической болезни. Кардиология. - 2002. - №7. - С.36-40.
5. Бранько В.В., Вахляев ВД, Богданова Э.А., Камшилина Л.С. Применение лазерной доплеровской флуометрии в кардиологии. Российский медицинский журнал. - 1998. -№3.-С.34-38.
6. Дегтярев В.А. Возможности комплексного исследования системы кровообращения у населения методом объемной компрессионной осциллометрии. Российские медицинские вести. - 2003. - №4. - С.18-28.
7. Маколкин В.И.,Подзолков В.И., Бранько В.В., Самойленко В.В., Абдуева Р.А., Булатов В.А. и др. Микруциркуляция в кардиологии. М., 2004. - 131 с.
Опубликовано: Сборник статей X межрегионального кардиологического форума «Неделя здорового сердца», Нижний Новгород, 15-18 мая 2006., стр 103-105